去年�����,來自麻省理工學(xué)院麥戈文腦科研究所的研究人員發(fā)現(xiàn)了III-E型CRISPR-Cas效應(yīng)蛋白Cas7-11并表征了它的特征��,它是**種能夠?qū)NA鏈進行**、有指導(dǎo)性的切割而在此過程中不傷害細胞的CRISPR 酶(Nature, 2021, doi:10.1038/s41586-021-03886-5)���。如今,在一項新的研究中����,他們與東京大學(xué)的合作者合作�,發(fā)現(xiàn)Cas7-11可以縮小到一個更緊湊的版本��,使其成為編輯活細胞內(nèi)RNA的一種更可行的選擇����。他們描述了這種新的��、緊湊的Cas7-11���,同時還對原始的Cas7-11進行了詳細的結(jié)構(gòu)分析�。
相關(guān)研究結(jié)果于2022年5月27日在線發(fā)表在Cell期刊上�,論文標(biāo)題為“Structure and engineering of the type III-E CRISPR-Cas7-11 effector complex”。論文通訊作者為麥戈文腦科研究所研究員Omar Abudayyeh�、麥戈文腦科研究所研究員Jonathan Gootenberg和東京大學(xué)研究員Hiroshi Nishimasu�����。論文**作者為麥戈文腦科研究所前博士后Nathan Zhou和東京大學(xué)的Kazuki Kato����。

Abudayyeh說,“當(dāng)我們觀察這種結(jié)構(gòu)時�,很明顯有一些不需要的部分��,我們實際上可以去除這些部分。這使得這種酶足夠小,以至于可以將它裝入在單一的病毒載體中進行**應(yīng)用?�!?
這些作者認為Cas7-11的新三維結(jié)構(gòu)是一種豐富的資源,可以回答有關(guān)這種酶的基本生物學(xué)問題��,并揭示未來調(diào)整它的功能的其他方法�����。
靶向RNA
在過去的十年里�����,CRISPR-Cas9基因組編輯技術(shù)使得科學(xué)家們有能力修改人類細胞內(nèi)的基因---這對基礎(chǔ)研究和逆轉(zhuǎn)致病性基因突變的**方法的開發(fā)都是一大福音。但是CRISPR-Cas9只對改變DNA起作用����,對于某些研究和臨床目的來說�,編輯RNA更為有效或有用�。
細胞終生保留它的DNA,并在復(fù)制時將一個相同的DNA拷貝傳遞給子細胞�,因此對DNA的任何改變都是相對長久性的�����。然而,RNA是一類更短暫的分子�����,由DNA轉(zhuǎn)錄而來����,并在不久后遭受降解���。
Gootenberg說��,“能夠長久地改變DNA有很多積極意義���,特別是當(dāng)涉及到**一種遺傳性基因**時�����。但是對于感染、受傷或其他一些暫時性的**來說,能夠通過靶向RNA來短暫地改變基因更有意義���。”
在Abudayyeh、Gootenberg和他們的同事發(fā)現(xiàn)Cas7-11并表征它的特征之前���,**能夠靶向RNA的酶會產(chǎn)生混亂的副作用;當(dāng)識別一種特定的基因時,這種稱為Cas13的酶開始切割它周圍所有的RNA�����。這一特性使得Cas13在診斷測試中很有效:它被用來檢測某個RNA片段的存在��,但對于需要有針對性切割的**方法來說���,它卻不是很有用�。
Cas7-11的發(fā)現(xiàn)為一種更**的RNA編輯形式打開了大門�,類似于用于DNA的Cas9酶。然而,巨大的Cas7-11蛋白太大,無法裝入單一的病毒載體中。
結(jié)構(gòu)上的新見解
為了解析出Cas7-11的整體結(jié)構(gòu)�����,Abudayyeh�、Gootenberg和Nishimasu使用了低溫電鏡技術(shù)���,這種技術(shù)將電子束照射在冷凍的蛋白樣本上��,并測量電子束的傳輸方式�。他們知道Cas7-11采用模塊化架構(gòu)����,由Cas7.1、Cas7.2�����、Cas7.3、Cas7.4�、Cas11���、INS和CTE這個結(jié)構(gòu)域和4個結(jié)構(gòu)域間接頭(linker)---L1����、L2�����、L3和L4---組成���,但是并不確定這些結(jié)構(gòu)域究竟是如何折疊和組裝在一起的����。
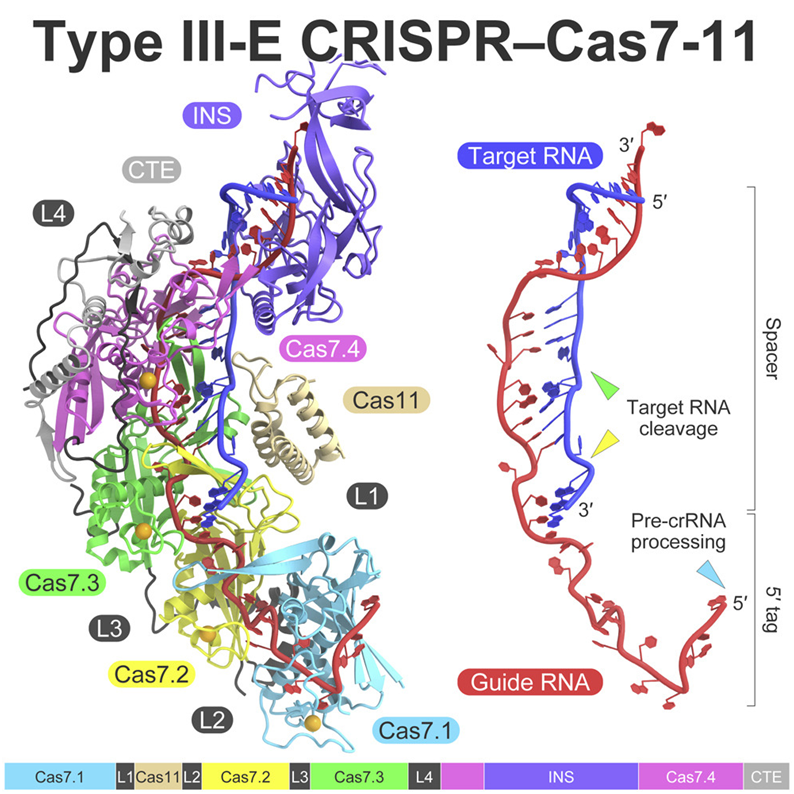
圖片來自Cell, 2022, doi:10.1016/j.cell.2022.05.003����。
Gootenberg說�,“從基本生物學(xué)的角度來看,Cas7-11真正迷人的地方在于它應(yīng)該是所有這些獨立的組成部分組合在一起�����,但它們卻融合成了一個基因�����。我們真的不知道為何會這樣�����。”
Cas7-11的結(jié)構(gòu)在是它結(jié)合它的目標(biāo)tRNA鏈和指導(dǎo)這種結(jié)合的向?qū)NA(gRNA)的過程中捕捉到的���,這揭示了它的這些組分部分是如何組裝的,以及它的哪些組分部分對于識別和切割RNA至關(guān)重要�����。這種結(jié)構(gòu)上的新見解對于弄清如何使Cas7-11在人體細胞內(nèi)執(zhí)行目標(biāo)任務(wù)至關(guān)重要�。
通過這種結(jié)構(gòu),這些作者發(fā)現(xiàn)Cas7-11通過使用Cas7.1結(jié)構(gòu)域?qū)⑺那绑wCRISPR RNA(pre-crRNA)加工成crRNA��,而且在crRNA的指導(dǎo)下�,它還使用Cas7.2和Cas7.3結(jié)構(gòu)域在兩個確定的位點上切割靶RNA。該結(jié)構(gòu)還揭示了Cas7-11的一個組成部分沒有任何明顯的功能作用�。這一發(fā)現(xiàn)表明他們員可以將這個組成部分移除��,重新設(shè)計Cas7-11,使它變得更小�����,而不影響它靶向RNA的能力����。Abudayyeh和Gootenberg測試了去除這個組成部分的不同片段的影響�,結(jié)果獲得Cas7-11的一個新的緊湊版本,被稱為Cas7-11S。有了Cas7-11S�,他們將它裝入在單個病毒載體中�,將它遞送到哺乳動物細胞中����,并有效地靶向目標(biāo)RNA。
這些作者目前正在計劃未來對Cas7-11來源**中與它相互作用的其他蛋白進行研究,并希望繼續(xù)致力于將Cas7-11用于**用途���。
Abudayyeh說,“想象一下,你可以有一種RNA基因療法��,當(dāng)進行**時�,它可以修改你的RNA,但當(dāng)你停止**時,這種修改就會停止��。這真地只是讓這組工具發(fā)揮作用的開始�����?�!?(生物谷 Bioon.com)
